DIFUSIÓN EN ESTADO NO ESTACIONARIO
En el mundo de la metalurgia, la Segunda Ley de Fick es la herramienta que nos permite "leer el futuro". Nos indica cómo los átomos de un elemento (como el Carbono) viajan al interior de un metal sólido y cómo su concentración cambia a medida que pasan las horas.
A diferencia de la difusión simple, aquí el tiempo es la clave: nada es estático.
1. La Ecuación Matemática del Cambio
Esta es la ecuación diferencial parcial que gobierna el proceso. No es solo un dibujo; cada parte representa un fenómeno físico:
Velocidad de cambio: Qué tan rápido se está acumulando el carbono en un punto específico a medida que el reloj avanza.
Coeficiente de Difusión: La "facilidad" con la que los átomos pueden saltar entre los espacios del metal. Depende de la temperatura.
Gradiente de concentración: La diferencia de "presión" química que empuja a los átomos de donde hay muchos a donde hay pocos.
Analogía para entenderlo:
Imagina una habitación llena de gente (concentración alta) y un pasillo vacío (concentración baja). Si abres la puerta, la gente empezará a fluir al pasillo. La Ley de Fick nos dice cuánta gente habrá en la mitad del pasillo después de 10 minutos.
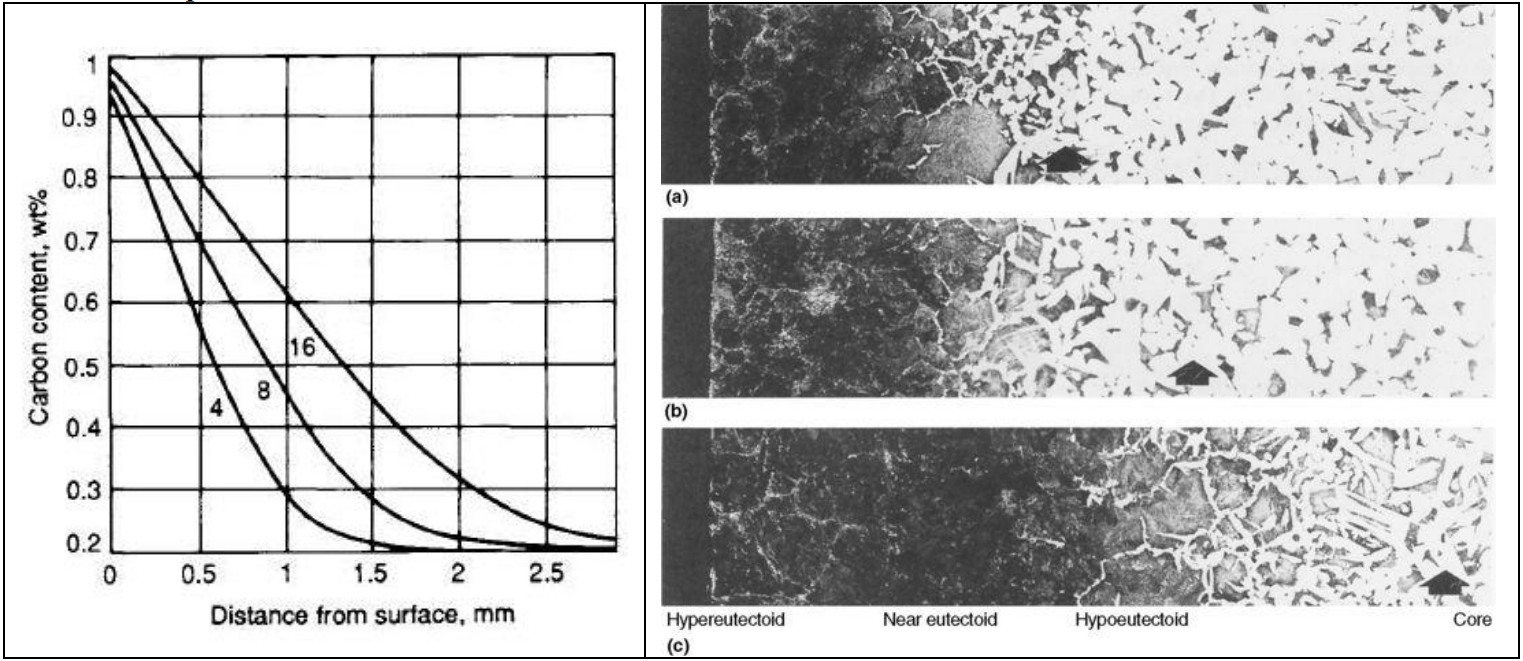
1. Comportamiento del Perfil de Concentración
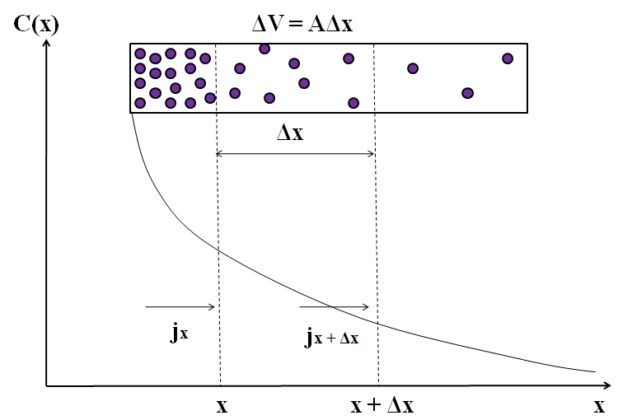
Figura 1. Grafica de la variacion de concentracion de soluto respecto a la distancia para diferentes tiempos de proceso.
Como se aprecia en la Figura 1, la curva siempre nace en la concentración superficial (Cs). A medida que el tiempo transcurre, el gradiente se suaviza y la profundidad de penetración aumenta. La forma de esta curva se describe matemáticamente mediante la función error gaussiana.
2. La Ecuación de Diseño Metalúrgico (Solución de Fick)
Cuando trabajamos con piezas industriales (como un engranaje en un horno de cementación), asumimos que la superficie está en contacto con un medio constante. Para este escenario, la Segunda Ley de Fick se resuelve mediante una función matemática específica que nos permite predecir la profundidad de la capa endurecida:
Mide qué tan cerca está el interior de la pieza (\(C_x\)) de saturarse completamente con el carbono del horno (\(C_s\)). Es un valor que va de 0 a 1.
La función erf (función error) modela la dificultad física que tienen los átomos para penetrar la red cristalina del metal a una profundidad \(x\).
Variables de diseño:
- \(x\): Profundidad desde la superficie (mm o m).
- \(t\): Tiempo de exposición en el horno (s o h).
- \(D\): Coeficiente de difusividad del material.
- \(C_s\): Potencial de carbono en la atmósfera.
Nota de Ingeniería: Esta ecuación asume que la pieza es lo suficientemente gruesa como para que el carbono nunca llegue al "otro lado" (modelo de sólido semi-infinito), lo cual es ideal para la mayoría de piezas mecánicas.
3. El "Traductor" entre la Teoría y la Práctica: Función Error (\(erf\))
La Función Error Gaussiana es el corazón del diseño metalúrgico. Como es una integral que no se puede resolver con una suma simple, los ingenieros usamos la Figura 2 como un "mapa de navegación".
Esta tabla nos dice: "Si quieres alcanzar este nivel de carbono (\(erf\)), debes penetrar hasta esta profundidad relativa (\(z\))".
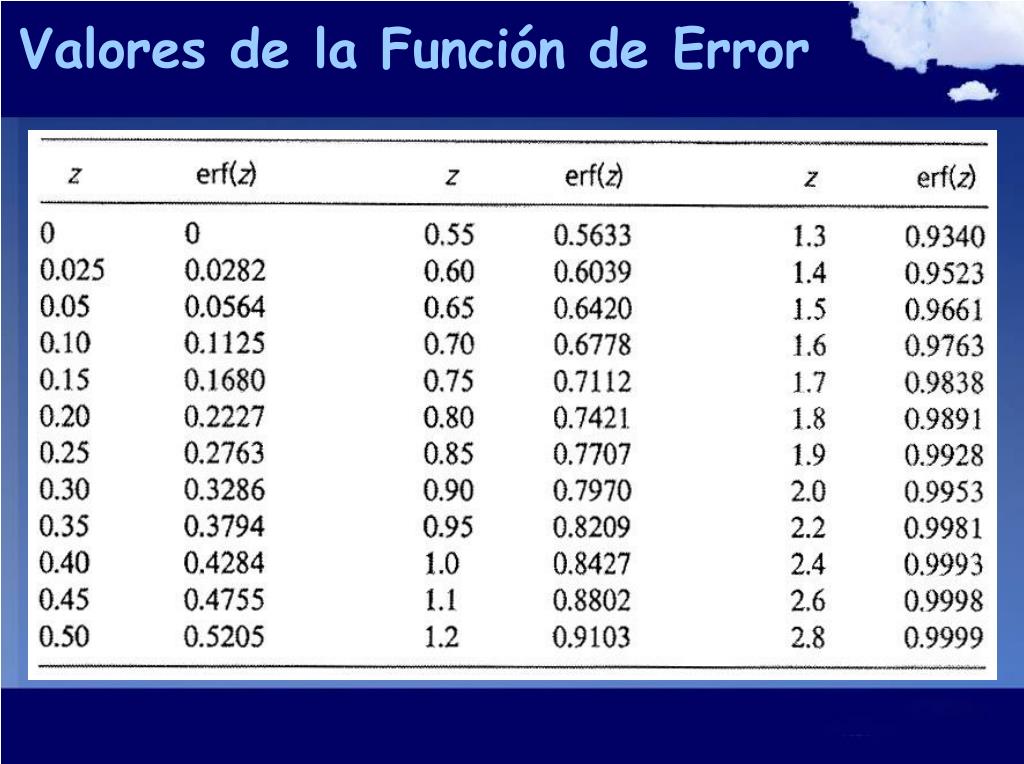
Figura 2. Diccionario de equivalencias entre el argumento \(z\) y la probabilidad de difusión \(erf(z)\).
Guía de Lectura Rápida
- 1 Entrada por Resultado: Si ya calculaste \(\frac{C_x - C_0}{C_s - C_0}\), busca ese número en las columnas de \(erf(z)\).
- 2 Salida por Posición: Una vez ubicado el valor, el número a su izquierda es tu \(z\). Este valor es el que usarás para despejar el tiempo o la profundidad.
- 3 Aproximación Lineal: Si tu valor está en medio de dos filas (ej. 0.45), toma el promedio de los valores de \(z\). ¡Así de simple!
Por qué usar la Tabla
Evita errores de redondeo y permite que cualquier persona, sin software avanzado, pueda diseñar un tratamiento térmico con precisión de laboratorio.
El error más común
No intentes multiplicar \(erf \times z\). Son una sola entidad. \(erf(z)\) es como decir \(\sin(45^\circ)\); no puedes separar la función del ángulo.
GUÍA MAESTRA: Resolución Completa
De la teoría al acero: resolvamos un caso real de ingeniería.
GUÍA MAESTRA: Resolución de Ejercicios
Ejemplo: Si el resultado es 0.4, este es tu número base.
CASO DE ESTUDIO: Cementación de un Engranaje
Un acero con 0.2% de C (C0) debe alcanzar 0.45% de C (Cx) a una profundidad de 0.5 mm. El horno tiene una atmósfera de 1.2% de C (Cs).
Paso 1: Preparar los "Ingredientes" (Datos)
Antes de calcular, asegúrate de que todo esté en las mismas unidades (Metros y Segundos).
Cs = 1.2
C0 = 0.2
Cx = 0.45
x = 0.0005 m (¡Ojo con los mm!)
Paso 2: Calcular la Relación de Concentración
Esto nos dice qué porcentaje del proceso de saturación hemos completado.
Paso 3: El Salto a la Tabla (La Función Error)
La fórmula dice: $Relación = 1 - erf(z)$. Por lo tanto:
Buscando en la Figura 2: Buscas 0.75 en la columna de la derecha. Verás que el valor más cercano nos da un z ≈ 0.81.
Paso 4: Despeje Final (Tiempo)
Igualamos nuestra z de la tabla con la fórmula de diseño:
Elevando al cuadrado y despejando t, obtenemos:
¡Felicidades! Has diseñado un tratamiento térmico. Si dejas la pieza 2 horas y 4 minutos en el horno, habrás cumplido con la especificación técnica de dureza a 0.5 mm.
3. El Pilar Científico: Diagrama Hierro-Cementita (Fe-Fe3C)
Sin este mapa, la difusión de carbono en el acero sería un proceso a ciegas.

Figura 3. Diagrama de fases Fe-C. Fuente: Blog de Metalografía UTP.
¿Por qué es vital para la Difusión?
El diagrama Fe-C nos dicta las reglas del juego. En un proceso de cementación, nos movemos principalmente en la región de la Austenita (Fase γ). Es aquí donde el hierro permite que los átomos de carbono se "hospeden" en sus espacios intersticiales y viajen hacia el núcleo de la pieza.
Régimen de Temperatura
Nos ayuda a identificar la Temperatura A3. Debemos trabajar por encima de esta línea para asegurar que la estructura sea completamente austenítica, optimizando la velocidad de difusión.
Potencial de Carbono (Cs)
El diagrama define el límite de saturación. A 1130°C, la austenita admite un máximo de ~1,76% de Carbono según el diagrama de ejemplo. Si el horno supera este límite, se formará Cementita Proeutectoide, fragilizando la superficie.
Estructura Final
Dependiendo de dónde terminemos en el diagrama tras la difusión, sabremos qué microestructura resultará al enfriar muy lentamente (Perlita) y este es el inicio para saber que sucederá al enfríarlo a diferentes Velocidades de enfriamiento (diagramas TTT y CCT). Con los cuales tendremos una idea de la dureza final.
Conclusión: El éxito de la cementación depende de cruzar la información del diagrama (límites de fase) con las Leyes de Fick (tiempo y profundidad). El diagrama nos dice "si es posible" y Fick nos dice "cuánto tarda".